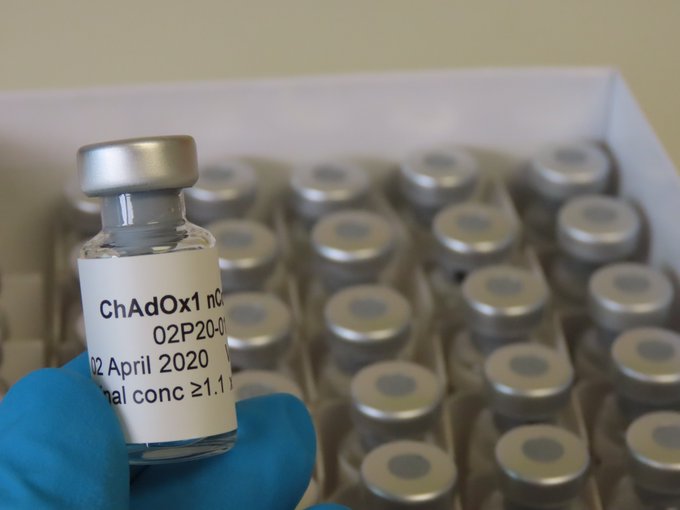
La farmacéutica AstraZeneca interrumpió el ensayo clínico de su vacuna contra el COVID-19 luego de que uno de los participantes sufriera “una enfermedad potencialmente inexplicable”, informó este martes 8 de septiembre un portavoz de la compañía a medios de comunicación estadounidenses.
“Esta es una acción de rutina que sucede siempre que hay una enfermedad potencialmente inexplicable en uno de los ensayos mientras se investiga, asegurándonos de que se mantiene la integridad de los estudios”, indicó el portavoz a la cadena Cnbc y al medio especializado Stat.
El voluntario que se enfermó reside en el Reino Unido, de acuerdo con Stat, que dijo desconocer la naturaleza de la reacción adversa que sufrió el individuo, aunque se espera que se recupere.
El portavoz de la farmacéutica, citado por medios locales, aseguró que se “está trabajando para acelerar la revisión de ese incidente único con el objetivo de minimizar cualquier impacto potencial en los planes del ensayo”.
AstraZeneca tenía previsto tener su vacuna disponible para el primer semestre de 2021. Es considerada una de las más avanzadas del mundo por la Organización Mundial de la Salud (OMS) y es una de las compañías con estudios en la fase III en EEUU, además de las farmacéuticas Pfizer y Moderna.
Esta es la primera vez que uno de esos ensayos para lograr la vacuna contra el COVID-19 tiene que ponerse en pausa por razones de seguridad.
La vacuna, llamada AZD1222 fue desarrollada por AstraZeneca y la Universidad de Oxford. Utiliza un virus modificado que no se replica y que funciona como agente para transportar genes derivados del nuevo coronavirus para que el cuerpo desarrolle una respuesta inmune.
Se encuentra desde finales de agosto en la fase III de los ensayos clínicos después de dar resultados positivos en mil personas en el Reino Unido en las primeras fases de los ensayos. En la fase III, la última antes de su aprobación, se probaría en 30.000 personas en Estados Unidos, Brasil y Sudáfrica.
Con información de EFE.